fosforiloiste on luminesenssi, joka tapahtuu kun energia toimittaa elektromagneettinen säteily, yleensä ultraviolettivaloa. Energialähde potkaisee elektronin atomi matalammasta energiatilasta "kiihtyneeseen" korkeamman energian tilaan; sitten elektroni vapauttaa energian muodossa näkyvä valo (luminesenssi), kun se laskee takaisin alhaisempaan energiatilaan.
Avaintyypit: fosforikeskus
- Fosforisenssi on eräs fotoluminesenssi.
- Fosforesenssissa materiaali absorboi valoa, mikä kohoaa elektronien energiatasot kiihtyneeseen tilaan. Valon energia ei kuitenkaan aivan vastaa sallittujen kiihtyneiden tilojen energiaa, joten absorboituneet valokuvat takertuvat triplettitilaan. Siirtymät alempaan ja vakaampaan energiatilaan vie aikaa, mutta kun ne tapahtuvat, valo vapautuu. Koska tämä vapautuminen tapahtuu hitaasti, fosforoiva materiaali näyttää hehkuvan pimeässä.
- Esimerkkejä fosforoivista materiaaleista ovat pimeässä hehkuvat tähdet, jotkut turvamerkit ja hehkuva maali. Toisin kuin fosforoivia tuotteita, fluoresoivat pigmentit lopettavat hehkua heti kun valonlähde on poistettu.
- Vaikka fosfori on nimeltään fosforielementin vihreällä hehkulla, se todella hehkuu hapettumisen vuoksi. Se ei ole fosforoiva!
Yksinkertainen selitys
Fosforikeskus vapauttaa varastoituneen energian hitaasti ajan myötä. Periaatteessa fosforoiva materiaali "varataan" altistamalla se valolle. Sitten energiaa varastoidaan tietyn ajan ja vapautetaan hitaasti. Kun energia vapautuu heti tapahtuneen energian absorboinnin jälkeen, prosessia kutsutaan fluoresenssi.
Kvanttimekaniikan selitys
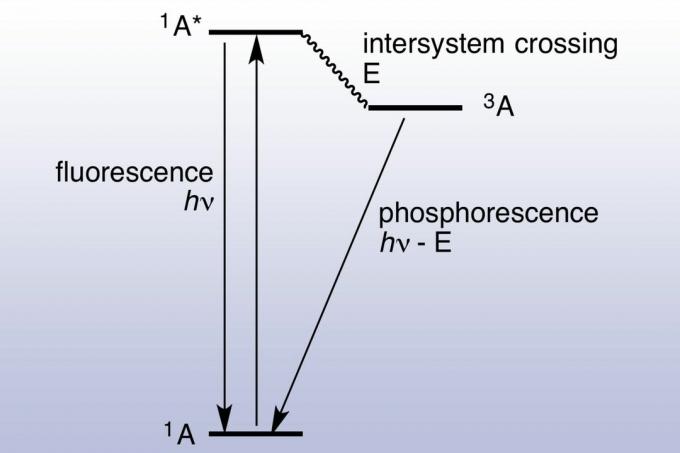
Fluoresenssissa pinta absorboi ja emittoi fotonin melkein heti (noin 10 nanosekuntia). Fotoluminesenssi on nopeaa, koska absorboituneiden fotonien energia vastaa materiaalien energiatiloja ja sallittuja muutoksia. Fosforikeskus kestää paljon kauemmin (millisekuntia päiviin), koska absorboitunut elektroni muuttuu viritetyksi tilaksi, jolla on suurempi spin-moninkertaisuus. Viritetyt elektronit jäävät loukkuun triplettitilassa ja voivat käyttää vain "kiellettyjä" siirtymiä pudotakseen pienemmän energian singletti-tilaan. Kvanttimekaniikka sallii kielletyn siirtymisen, mutta ne eivät ole kineettisesti suotuisia, joten niiden esiintyminen vie kauemmin. Jos valoa absorboidaan tarpeeksi, varastoidusta ja vapautetusta valosta tulee riittävän merkittävää, jotta materiaali näyttää "hehkuvan tumma. "Tästä syystä fosforoivat materiaalit, kuten fluoresoivat materiaalit, näyttävät erittäin kirkkaalta mustassa (ultraviolettivalossa). Jablonskin kaaviota käytetään yleisesti fluoresenssin ja fosforesenssin välisen eron näyttämiseen.
Historia
Fosforoivia materiaaleja koskeva tutkimus on peräisin ainakin vuodelta 1602, kun italialainen Vincenzo Casciarolo kuvaili "lapis solaris" (aurinkokiveä) tai "lapis lunaris" (kuukivi). Löytö kuvailtiin filosofian professori Giulio Cesare la Gallan kirjassa 1612 De Fenomenis Orbe Lunaessa. La Galla kertoo, että Casciarolon kivi säteili siihen valoa, kun se oli kalsifioitunut lämmityksen avulla. Se sai valoa auringolta ja sitten (kuten Kuu) antoi valoa pimeässä. Kivi oli epäpuhdasta bariittiä, vaikka myös muut mineraalit osoittavat fosforointia. Niihin kuuluu joitain ruutu (jonka Intian kuningas Bhoja tunsi jo 1010-1055, Albertus Magnus löysi uudelleen ja Robert Boyle löysi uudelleen) ja valkoinen topaasi. Erityisesti kiinalaiset arvostivat tyyppiä fluoriittia, nimeltään klorofaani, joka osoittaisi luminesenssia kehon lämmöltä, valolle altistumiselta tai hieromista. Kiinnostus fosforesenssin ja muun tyyppisen luminesenssin luonteeseen johti lopulta radioaktiivisuuden löytämiseen vuonna 1896.
tarvikkeet
Muutamien luonnollisten mineraalien lisäksi fosforointia tuottavat kemialliset yhdisteet. Luultavasti tunnetuin näistä on sinkkisulfidi, jota on käytetty tuotteissa 1930-luvulta lähtien. Sinkkisulfidi emittoi yleensä vihreän fosforin, vaikka fosforia voidaan lisätä valon värin muuttamiseksi. Fosforit absorboivat fosforesenssin lähettämää valoa ja vapauttavat sen sitten toisena värinä.
Viime aikoina strontiumaluminaattia käytetään fosforointiin. Tämä yhdiste hehkuu kymmenen kertaa kirkkaammin kuin sinkkisulfidi ja varastoi myös energiansa paljon kauemmin.
Esimerkkejä fosforoinnista
Yleisiä esimerkkejä fosforoinnista ovat tähdet, joita ihmiset asettavat makuuhuoneen seinille, jotka hehkuvat tuntien ajan sen jälkeen, kun valot ovat sammunut, ja maalauksen, jota käytetään hehkuvien tähden seinämaalausten tekemiseen. Vaikka elementti fosfori hehkuu vihreänä, valo vapautuu hapettumisesta (kemiluminesenssi) ja on ei esimerkki fosforesenssista.
Lähteet
- Franz, Karl A.; Kehr, Wolfgang G.; Siggel, Alfred; Wieczoreck, Jürgen; Adam, Waldemar (2002). "Luminesoivat materiaalit" Ullmannin kemian tietosanakirja. Wiley-VCH. Weinheim. doi: 10.1002 / 14356007.a15_519
- Roda, Aldo (2010). Kemiluminesenssi ja bioluminesenssi: menneisyys, nykyisyys ja tulevaisuus. Kuninkaallinen kemian yhdistys.
- Zitoun, D.; Bernaud, L.; Manteghetti, A. (2009). Pitkäkestoisen fosforin synteesi mikroaaltouunilla. J. Chem. Educ. 86. 72-75. doi: 10.1021 / ed086p72